日前,由北京大学魏文胜教授领衔的研究团队,基于circRNA技术开发的新冠疫苗,在小鼠和恒河猴实验中都诱导出了有效的免疫应答,并且能够针对不同的新冠病毒变种包括德尔塔(Delta)和奥密克戎(Omicron)提供保护。该项研究在知名学术期刊《细胞》在线发表,可谓一石激起千层浪。 作为近几年兴起的突破性技术,mRNA疫苗通过脂质纳米颗粒(LNP)将mRNA导入体内来表达抗原蛋白,以刺激机体产生特异性免疫反应。新冠肺炎疫情(COVID-19)爆发后,针对性的mRNA疫苗在多种疫苗类型中脱颖而出。与此同时,诸如自复制mRNA和circRNA等新型路线也逐渐走入大众视野。 circRNA分子呈共价闭合环状结构,不含5’-Cap和3’-polyA结构,不易被RNase降解,具有较高的稳定性。魏教授团队采用了Group I核酶自催化策略来产生编码SARS-CoV-2 RBD抗原的circRNA。该种方法是将核心序列插入到环化载体,生成用于体外转录(IVT)的模板,产生线性RNA后通过Group I核酶自催化形成circRNA。在RNA环化后需要用RNase R对未环化的RNA进行消化,来达到分离circRNA的目的。
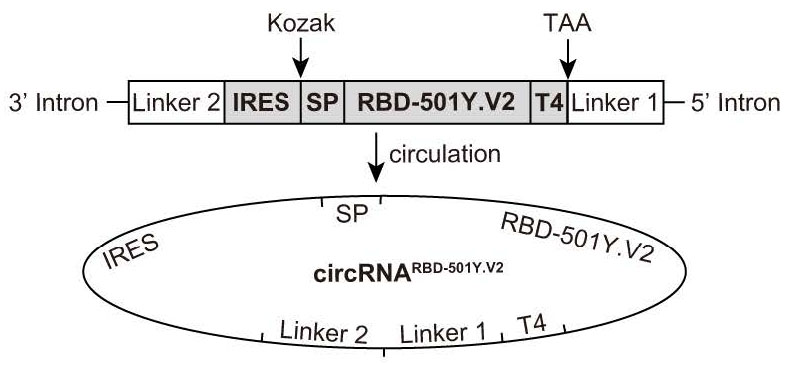
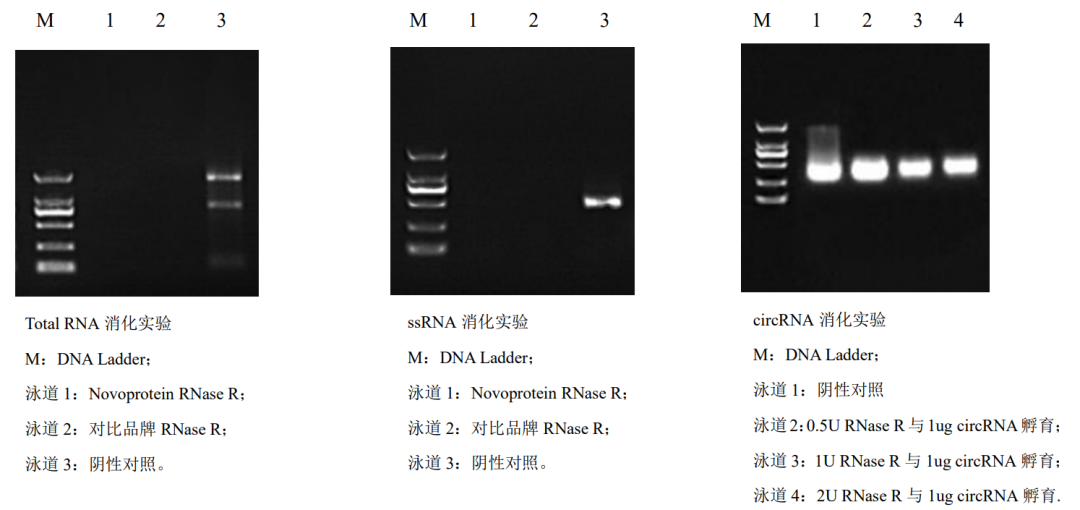
。 RNase R针对Total RNA、ssRNA及circRNA的消化实验,实验证明, RNase R可以消化绝大部分的总 RNA样品,完全消化ssRNA样品,对circRNA样品起到良好的纯化效果。
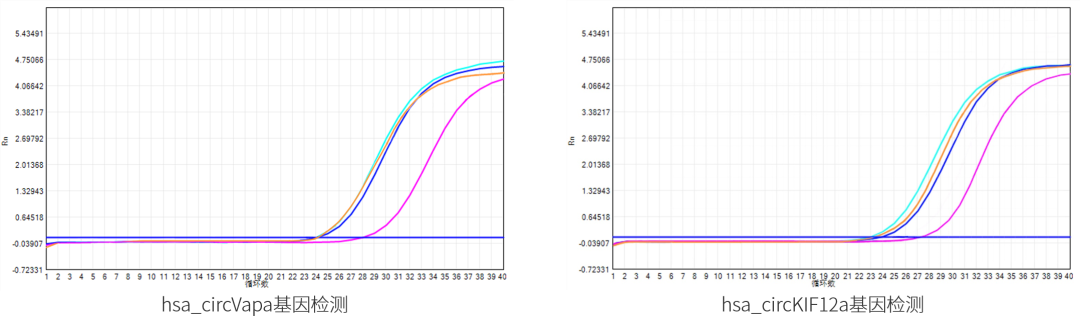
为了进一步验证RNase R对环状RNA无酶切作用,利用qPCR方式检测经RNase R(蓝色:近岸蛋白;绿色:对照品牌)消化后的总RNA样品中hsa_circKIF12a和hsa_circVapa基因的丰度变化,结果显示,与阴性组(橙色)相同,两个基因的丰度基本没有变化,而经RNase A(粉色)消化的样品中基因丰度明显下降,表明环状RNA耐受RNase R的消化。
circRNA在生物和生物医学领域的研究越来越热,环状RNA被证实具有多种分子机制,包括调控基因的转录和翻译,调控蛋白质互作甚至可以被翻译成小肽。不仅如此,环状RNA还具有转化医学价值,它们在作为诊断性生物标志物或疾病治疗靶点方面都具有应用潜力。在利用体外环化RNA技术制备针对免疫性疾病或癌症的环状RNA药物方面,也逐步有企业加入进来,目前国内外已有数十家企业布局circRNA技术路线。相信随着研发推进,circRNA技术会迎来新一波研究和产业化热潮。
相关产品
| 货号 | 产品名称 |
| E224 | RNase R |
| E131 | T7 High Yield RNA Transcription kit |
| GMP-E121 | T7 RNA Polymerase, GMP Grade |
| GMP-E125 | RNase Inhibitor, GMP Grade |
| GMP-M036 | Pyrophosphatase, Inorganic (yeast), GMP Grade |
苏州近岸蛋白质科技股份有限公司,是一家专注于重组蛋白应用解决方案的高新技术企业,主营业务为靶点及细胞因子类蛋白、重组抗体、酶及试剂的研发、生产和销售,并提供相关技术服务。公司定位为医疗健康与生命科学领域原料与技术解决方案的上游供应商,致力于为下游客户提供及时、稳定、优质的产品及服务,助力全球生物医药企业和研究机构的技术与产品创新升级。
详询www.novoprotein.com.cn或致电400-600-0940。
