糖尿病是因胰岛素绝对或相对分泌不足以及靶组织细胞对胰岛素敏感性降低引起蛋白质、脂肪和电解质等一系列代谢紊乱综合征,以高血糖为主要标志。糖尿病的一个主要特征是功能性β细胞不足,因此诱导β细胞的复制或者保护现有β细胞以增加β细胞的数量是糖尿病治疗策略之一。氧化应激是β细胞糖毒性的重要媒介,有研究表明β细胞长期暴露在高水平活性氧(ROS)条件下会导致功能性β细胞数量减少。因此,调节ROS平衡对于维持糖尿病患者的功能性β细胞数量起到至关重要的作用。
Nrf2是一种转录因子,可以保护细胞免受氧化应激反应。通常情况下,Nrf2与抑制因子如Keap1结合,处于未激活状态,Nrf2泛素化进而降解。氧化应激时,Keap1氧化使得对Nrf2的靶向结合能力下降,从而Nrf2激活并转移至细胞核与ARE结合,激活下游基因的转录,翻译成蛋白,从而发挥生理功能。有研究报道,KEAP1与NRF2这对组合与多种疾病的发生有关系,包括糖尿病、癌症、神经退行性疾病在内的多种慢性疾病。
2022年3月,Diabetes杂志发表的了美国Donald K. Scott研究团队的工作 “
Nrf2 Regulates β-Cell Mass by Suppressing β-Cell Death and Promoting β-Cell Proliferation” 。该研究发现Nrf2是维持β细胞氧化还原平衡和生存所必需的,Nrf2激活可以驱动啮齿动物和人类β细胞增殖。该研究揭示了葡萄糖在INS1细胞和原代β细胞中可以快速激活Nrf2;Nrf2在葡萄糖刺激的β细胞增殖以及适应性β细胞增殖、适应性β细胞质量的扩大和保护小鼠避免细胞死亡中发挥重要作用;Nrf2在维持胰岛素水平过程中发挥重要作用;Nrf2的激活增加HFD饮食小鼠β细胞增殖和β细胞质量改善糖耐量,并且Nrf2可以提高人β细胞的增殖。
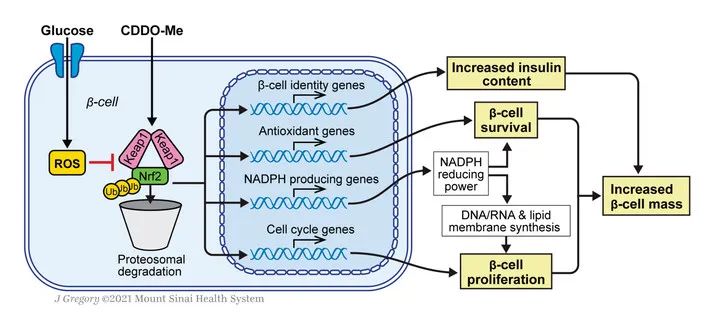
基于Nrf2可以保护β细胞避免受高脂肪饮食后导致的细胞凋亡,激活Nrf2可以增加β细胞的增殖和数量提高葡萄糖耐受能力,研究人员将人胰岛移植至小鼠肾包膜下,并利用Nrf2激活剂CDDO-Me进行治疗,发现可以同时提高人和小鼠β细胞增殖能力与胰岛素分泌能力。
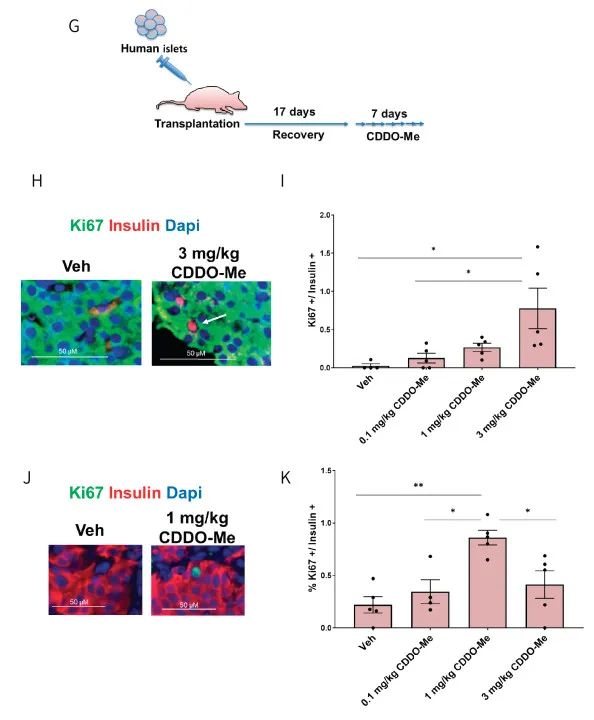
文本的发现提示,Nrf2保护和扩大β细胞质量可能是一个潜在的糖尿病治疗靶点及方案。
原文链接:
https://diabetesjournals.org/diabetes/article/71/5/989/144597/Nrf2-Regulates-Cell-Mass-by-Suppressing-Cell-Death
