mRNA疫苗生产过程中,质粒线性化因其相对稳定和成熟的放大生产工艺等优势成为主流的模板制备方式。在质粒线性化过程中,要求酶切产物必须为5’端突出或平末端,因为如果酶切产生3’突出末端的模板,在体外转录(IVT)时,就会增加副产物dsRNA的产生风险,而dsRNA是一类免疫反应的强刺激物,需要严格控制,才能保证mRNA疫苗的有效性。因此,酶切效率高,可以产生5’端突出或平末端,且不易在目标序列内出现酶切位点的限制性内切酶,成为mRNA模板制备的必备品之一。
经过不断验证与探索,近岸蛋白在原有限制性内切酶产品基础上,再次推出无动物源性PmeI酶。PmeI酶克隆自门多萨假单胞菌(Pseudomonas mendocina)PmeI基因,其识别位点长达8个碱基,极不容易在目标序列中出现相同酶切位点,实现高效质粒线性化,同时,其产生的线性化质粒为平末端。
5' G T T T ↓ A A A C 3'
3' C A A A ↑ T T T G 5'
PmeI酶切识别位点
有效切割质粒及PCR产物片段
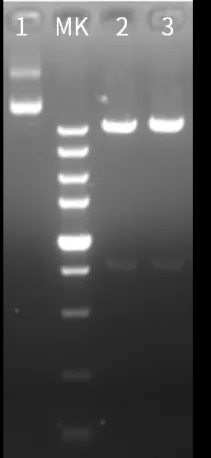 |
50μl反应体系中,不同品牌PmeI与1µg 质粒进行双酶切(质粒序列中含有两个PmeI酶切位点),37℃孵育1h,质粒被完全线性化。 1:阴性 MK:DNA Marker 2:品牌A 3:Novoprotein |
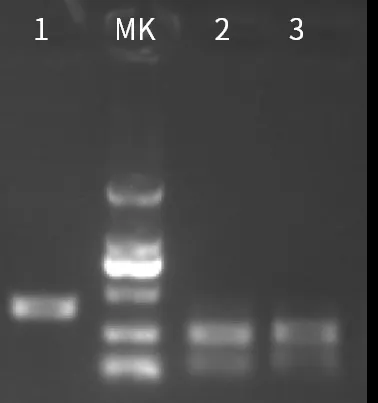 |
50μl反应体系中,不同品牌PmeI与0.5µg短片段(375bp),37℃孵育1h,片段被完全切割。 1:阴性 MK:DNA Marker 2:品牌A 3:Novoprotein |
更多主流限制性内切酶还有酶切后形成5’末端突出结构的XbaI酶,以及IIS型限制性内切酶BspQI、BsaI,其酶切位点在识别位点以外,酶切后可将Poly A结构直接暴露在3’端而不产生冗余的酶切位点残基,从根本上杜绝多余碱基造成的不确定性。
|
5'...T↓CTAGA...3' 3'...AGATC↑T...5' Xbal酶切识别位点 |
5'...GCTCTTC(N)1↓...3' 3'...CGAGAAG(N)4↑...5' BspQI酶切识别位点 |
5'...GGTCTC(N)1↓...3' 3'...CCAGAG(N)5↑...5' Bsal酶切识别位点 |
近岸蛋白在推动mRNA疫苗研发生产过程中不断探索创新,GMP级限制性内切酶BsaI、BspQI和XbaI,无动物源性PmeI,为客户提供更多的酶切位点选择。
相关产品