*文章转载自求实药社
ING 2021 第四届免疫及基因治疗论坛组委会有幸邀请到IsoPlexis亚太区应用经理 李倩博士基于IsoPlxis分析平台的优势,以采访形式分享了对单细胞蛋白质组学未来的发展前景与应用前景的看法、IsoPlexis对单细胞蛋白质学技术研发难点的见解、单细胞多组学分析技术对肿瘤免疫治疗提供的几点新思路和解决方案等内容。
李倩博士
IsoPlexis
亚太区应用经理
李倩博士毕业于北京大学医学部免疫学专业,研究方向主要为抑癌基因对T细胞和B细胞发育及免疫功能的影响。目前担任IsoPlexis公司亚太区应用经理,支持单细胞功能蛋白质组学分析平台的转化应用,她拥有丰富的免疫学、肿瘤学、细胞生物学等领域的应用经验,为许多科研及工业用户提供应用支持和整体解决方案,包括细胞治疗、生物制药、肿瘤免疫研究等领域。在加入IsoPlexis前,她曾供职于德国美天旎和赛多利斯公司,拥有多年从业经验,负责多种高通量细胞分析、细胞分选和原代样本处理等细胞相关产品的技术支持工作。
Q:据统计,过去10年间,对于单细胞蛋白质组学的热议一直不断,大家对于单细胞蛋白质组学的热情也只增不减,您是如何看待单细胞蛋白质组学未来的发展前景与应用前景?
目前单细胞蛋白质组学技术主要应用于肿瘤免疫、细胞治疗、炎症、自身免疫性疾病、干细胞、神经系统疾病等领域,随着检测蛋白指标种类的完善和数量的增加,未来将可能应用到越来越广阔的研究领域。
实际上,与流式细胞技术和单细胞测序相比,单细胞蛋白质组学技术目前仍处于起步阶段,作为单细胞多组学技术的一个重要补充,相信未来将会更多地与其他单细胞技术进行联合应用,以获得更丰富和深入的多组学信息,如探讨转录组水平和蛋白水平之间的调控机制,帮助探讨生物发育和疾病发生机制,为药物开发提供更多依据。
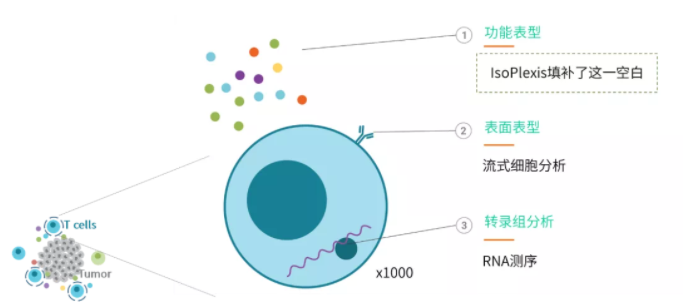
单细胞功能蛋白组学提供单细胞功能表型信息
随着微流控、光学检测、生物物理和电子工程等其他技术的创新,我们有理由相信单细胞蛋白质组学检测技术将有更多的突破,如实现更高的通量、更高的单细胞捕获效率、更高的灵敏度以及更丰富的检测指标和组合,随着这些方面的改进及应用普及,检测成本也将大大降低,让更多的实验室可以无负担的使用该技术进一步推动研究进展。
Q:请您简单介绍一下IsoPlxis的单细胞功能蛋白质组学分析平台,与其他分析平台相比,IsoPlxis的分析平台有何优势?
Isoplexis单细胞功能蛋白质组分析平台采用微流控技术,通过IsoCode芯片上的12,000个独立的亚纳升级别的微室同时捕获上千个单细胞,搭配IsoCode芯片抗体条形码技术,可以捕获每个小室中单个活细胞分泌的多重蛋白质,或者对单细胞裂解后释放出的多重磷酸化蛋白进行捕获,然后通过基于荧光ELISA原理的全自动化蛋白检测技术,捕获多重蛋白的荧光信号,一次可检测多达30种以上的蛋白质。在检测中从每个单细胞获得的蛋白质组信号将无缝传输到IsoSpeak生信分析软件,进行全自动分析和可视化数据呈现,得到的图表可直接用于文章发表。
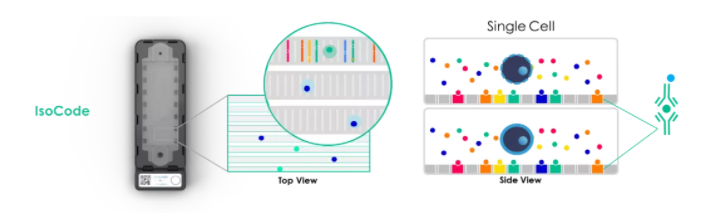
单细胞功能蛋白组检测原理示意图
与其他分析平台相比,IsoPlexis的单细胞功能蛋白质组学分析平台聚焦在细胞功能的分析上,且可以提供传统分析方法无法实现的单细胞分辨率。它以独有的单细胞分泌蛋白组分析群体细胞中真正发挥关键作用的多功能细胞亚群,如在疾病中发挥重要保护作用的超级细胞亚群以及损伤机体的不良细胞亚群,从而展示出新的生物学新价值,即与临床治疗结局建立相关性。我们目前已经创建了50 多个数据集,可以在临床前期从预测的角度揭示具有更持久疗效的最佳免疫联合疗法、细胞治疗或疫苗候选物。在临床阶段,我们展示了PSI作为一种新型生物标志物用于预测患者临床缓解,以实现更好的精准治疗。

此外,IsoPlexis单细胞磷酸化蛋白质组学可以对细胞内信号通路相关的多重磷酸化蛋白进行检测,并在当天获得结果。在传统方法中,磷酸化蛋白被用于鉴定单个蛋白质的功能,而没有关于它们如何协同作用的见解。IsoPlexis单细胞磷酸化蛋白质组能够提供整个蛋白质信号传导通路的背景信息,从而揭示整体信号网络如何运作,让研究人员可以更好地了解异常细胞的下游效应,更好地评估癌症靶向治疗疗效,将免疫治疗和靶向治疗推进到一个更加精确和个性化的阶段。
目前我们提供IsoLight、IsoSpark和IsoSpark Duo三款型号的设备,实现不同检测通量的需要。同时,我们已经在北京、上海、深圳设立合作实验室,提供对外实验测试服务,让感兴趣的研究人员可以先行体验单细胞蛋白质组技术![]()
![]()

Q:单细胞蛋白质学技术在研发过程中,存在哪些技术难点亟待解决?IsoPlexis作为一家单细胞多重功能蛋白质检测解决方案的供应商,对这些技术难点有何独特见解?
首先,我们来解析下单细胞功能蛋白质组学技术。主要可以从两个层面来看,一个是单细胞层面,由于细胞群体样本具有很大异质性,比如肿瘤细胞、免疫细胞、干细胞等,即使是表型完全一致的细胞亚群在功能层面上细胞之间也存在较多差异。传统的检测方法只能检测相关样品中分泌到溶液中的各类蛋白的平均浓度,这是诸多细胞和组织的共同分泌的结果,只能得到被平均化的结果,往往与后期实验结果、筛选目标细胞类群、分析免疫治疗产品效能和预测患者治疗效果等方面的相关性较差,极大地限制了相关研究和应用转化。
表型相似的细胞可能功能差异

![]()
第二个是蛋白质层面,目前的单细胞技术包括细胞表型分析,如流式细胞分析技术,基因组层面的单细胞分析,如单细胞基因组、转录组、表观遗传组等,也是近几年非常受到关注的技术。而单细胞蛋白组层面的分析技术可以从功能层面对现有的单细胞技术进行补充,从而与体内生理学及临床应用建立相关性,这方面的技术目前还是比较稀少的。
这个技术的难度在于如何在单细胞的层面实现多重功能蛋白质的检测,单细胞蛋白检测势必要求比较高的灵敏度,而同时检测多种蛋白则对所使用的捕获抗体和检测抗体提出了更高的要求,以避免产生相互信号干扰。现如今的蛋白检测方法要么在通量上寻求突破,要么在检测灵敏度上追求极限,很难做到二者的兼顾。
另外,如何选择检测蛋白的种类以反映细胞的真实功能也是需要考量的因素,包括细胞在外界刺激下分泌的蛋白及胞内信号通路激活涉及的磷酸化蛋白等。参与生物反应和行为的蛋白种类多达数百种,如何从中选出有代表性的蛋白指标,尽量降低检测成本,同时能综合反应细胞对外界不同刺激条件或药物处理后的反应,需要大量的前期数据积累和反复验证。
最后,基于单细胞蛋白质组学获得的大量生物学信息,如何将它转化为可指导下一步决策的定量指标,获得有意义的数据也是非常重要的。在当今的大数据时代,获得海量数据不再困难,而要从大数据中搜索出有效信息,则是目前面临的一个新挑战。
Q:IsoPlexis单细胞蛋白组技术使用了一种综合的评价标尺——细胞多功能指数(PSI),对细胞的功能进行表征。请您再详细介绍一下PSI在CART细胞治疗中是如何应用的?
在CAR-T细胞治疗中,IsoPlexis单细胞蛋白组学分析有着非常广泛的应用。它通过对CAR-T细胞在抗肿瘤应答过程中分泌的多种细胞因子进行单细胞维度的分析,从而鉴定出在整个CAR-T细胞群体中真正发挥强大作用的其中一部分CAR-T细胞亚群,亦即可分泌两种或以上细胞因子的细胞,我们称之为多功能细胞,这部分细胞可能只占整个细胞群体的20%,甚至更少,而多项研究证实,这群细胞的存在与CAR-T细胞治疗病人的疗效有着显著相关性。衡量这群多功能细胞效应的指标我们叫做“细胞多功能指数(polyfunctional strength index, PSI)”。
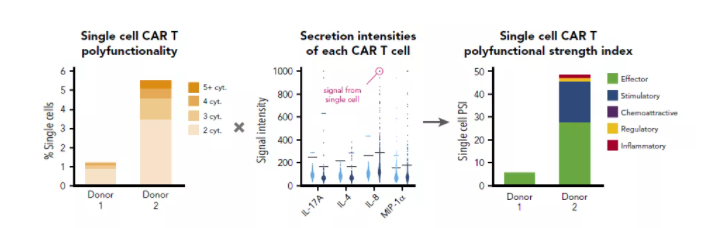
因此,IsoPlexis单细胞功能蛋白组学分析平台通过评估免疫细胞应答情况,可用于细胞治疗产品回输病人前的质量评估和疗效预测,在研发中可用于鉴定具有更高功效和更低免疫毒性的细胞治疗产品,从而助力细胞治疗产品的开发,实现更好的精准医疗。
早在2018年,Kite Pharma就在《Blood》上发表了CD19 CAR-T产品治疗非霍奇金淋巴瘤的一期临床试验数据,其中采用单细胞蛋白质组学技术检测到CAR-T细胞产品回输前的PSI与治疗后癌症患者的客观缓解呈统计学显著相关性。研究人员同时也使用了流式细胞分析技术和ELISA检测CAR-T产品的细胞表型和细胞因子分泌情况,但只有单细胞蛋白质组学分析能在这项血液瘤临床试验中区分出该细胞治疗产品的有效者和无效者。
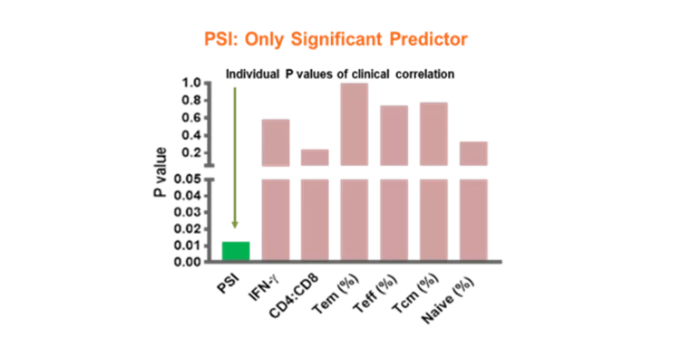
在2021年7月最新发表在《Nature Medicine》上的一篇关于双特异性CD19/CD22 CAR-T细胞治疗复发和难治性B细胞肿瘤的一期临床试验中也用到单细胞蛋白质组学技术比较双特异性CAR-T细胞在不同靶抗原刺激产生的T细胞应答强弱,以及与单特异性CAR-T细胞相比的效力,以此去探讨肿瘤抗原逃逸引起的疾病进展/复发的作用机制。这篇文章显示CD19抗原丢失是导致CD19 CAR-T细胞耐药的主要原因,突出了跨靶点设计具有同等效力的多特异性CAR-T细胞的挑战,并确定细胞因子的产生可作为CAR - T细胞效力的一个重要质量指标。

除了CAR-T细胞治疗,在其他类型的细胞治疗中,如TCR-T、TIL、CAR-NK等细胞治疗,IsoPlexis单细胞蛋白组学技术也有越来越多的应用,敬请大家继续关注。
Q:由于单细胞蛋白组学研究的发展,促进了科研人员对于单细胞转录组学与单细胞蛋白组学联合分析等单细胞多组学助力免疫治疗的研究工作,单细胞多组学分析技术会对肿瘤免疫治疗提供哪些新思路和解决方案?
单细胞多组学包括细胞层面、基因层面和蛋白层面的单细胞分析,每个维度提供的信息可互相补充,帮助进一步加深对免疫作用机理的探索,推进抗肿瘤研究及治疗开发。目前在免疫治疗领域,已有多项研究及临床试验数据证实,单细胞蛋白质组学技术可用于免疫相关治疗的体外疗效评估,以及预测病人的临床结局,包括基于PD-1抗体的联合免疫疗法、双特异性抗体、细胞治疗(CAR-T)、肿瘤疫苗开发等。
比如在2021年7月,来自德克萨斯大学安德森癌症中心的Adi Diab博士课题组,在《Journal of Clinical Oncology》期刊上发表了题为“Bempegaldesleukin Plus Nivolumab in First-Line Metastatic Melanoma”的文章。作者在利用单细胞蛋白质组学技术对患者治疗前后外周血中T细胞和NK细胞的单细胞多功能强度指数(PSI)进行了分析,发现CD8+细胞的PSI增加与患者客观缓解改善呈正相关,通过这一生物标志物可以让研究人员比以前的传统技术更早地评估患者对纳武单抗/BEMPEG联合治疗的反应。此外,在为期3年的随访中,治疗前后CD8+ PSD(PSI差异)高的患者表现出更高的客观缓解率,或治疗结果改善,这突出了PSI作为一种与患者缓解呈正相关的预测性生物标志物的潜力。

