Cre/loxP系统简介
来源于噬菌体P1的Cre/loxP系统主要包括2个重要组成部分:一个是loxP位点,另一个就是可以对loxP位点进行识别的Cre酶,可以实现对目的基因删除、翻转、易位和序列互换。利用特异性的启动子使Cre酶在特异性的组织器官表达,实现对特定的组织或细胞的基因的操作,同时可以在Cre/loxP体系中添加ERT2,实现在特定时间对目的基因的操作。(更多Cre体系相关内容,可参考【知识分享】一半海水、一半火焰,分子表达操控中高频出现的Cre、Flp、Dre等重组酶系统如何工作)
病毒载体介导的Cre/loxP系统,除了具备以上特点之外,相较于转基因小鼠,可以大大缩短实验的周期。另外,多种多样的病毒载体,可以最大限度的满足各类实验的需求。各类病毒载体的特点如下:
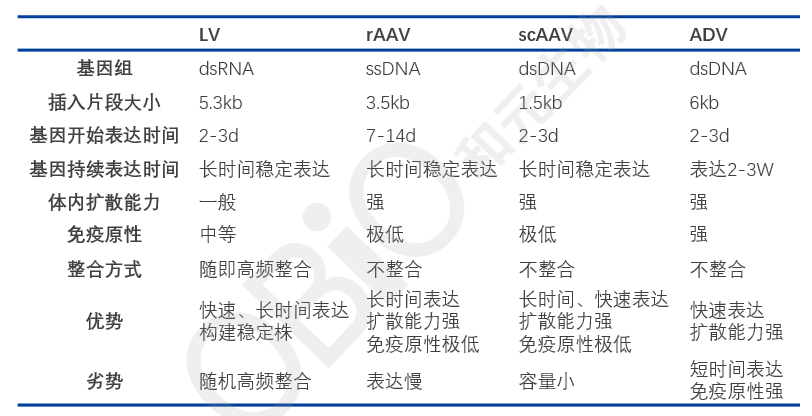
病毒载体介导的Cre/loxP系统应用案例
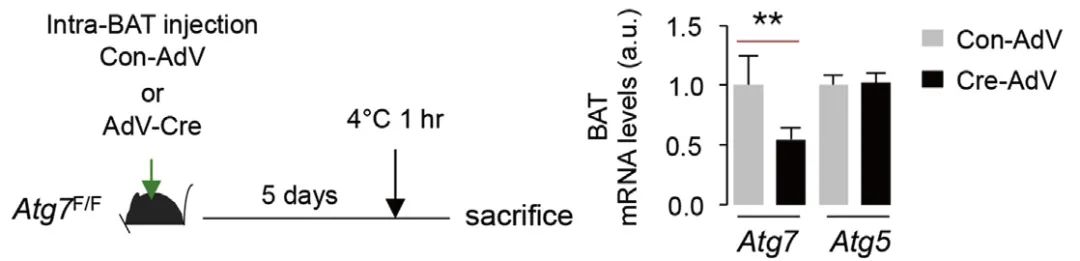
利用ADV介导的Cre体系可以实现对特定组织器官的快速敲除。美国爱因斯坦医学院的Rajat Singh团队[1],利用ADV载体携带Cre酶基因,注射到Atg7f/f工具鼠棕色脂肪组织,对脂肪组织Atg7基因进行编辑,5天后对Atg7表达进行分析,Atg7显著减少。
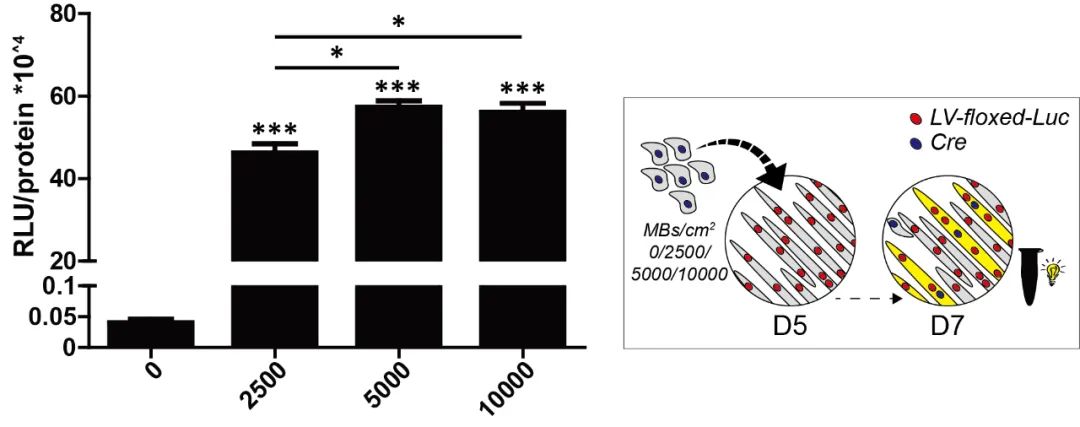
利用LV介导的Cre体系整合至基因组的特性,可以实现稳定细胞株的构建。荷兰马斯特里赫特大学医学中心Anita Kneppers研究团队[2],利用LV病毒载体构建了一种基于Cre/loxP的细胞融合报告体系,实现成肌细胞-肌管融合后荧光素酶的条件表达。
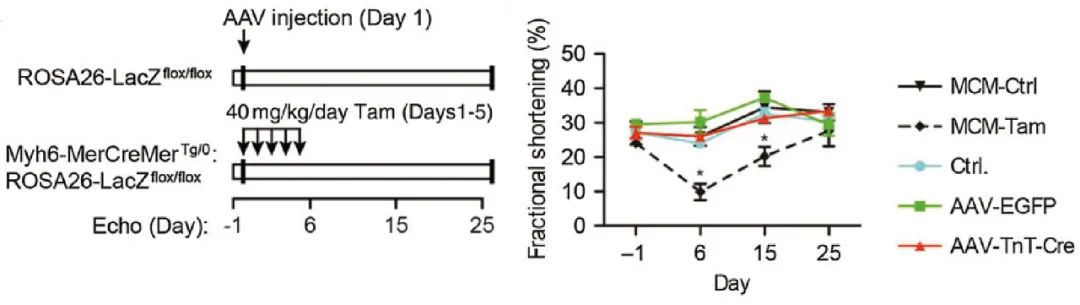
rAAV具有免疫原性低、多血清型、长时间表达等特点,在体内研究中广泛应用。德国慕尼黑大学Oliver J. Muller 研究团队[3]利用AAV-TnT-Cre特异性对成年小鼠心脏的基因进行敲除,从而替代MerCreMer-Tamoxifen体系,避免Tam对心脏功能产生的副作用。
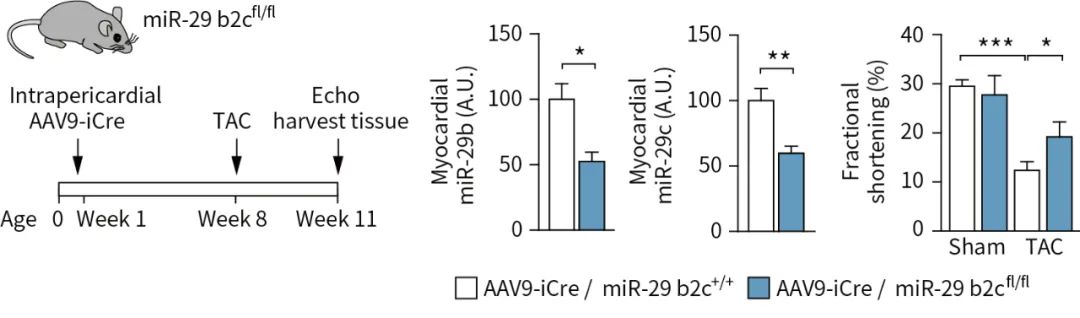
scAAV即自互补AAV,弥补了rAAV病毒载体表达较慢的缺点,感染3天后即可表达,同时可长时间稳定表达。德国慕尼黑工业大学Stefan Engelhardt研究团队[4],利用scAAV-iCre对miR-29 b2cfl/fl 小鼠心肌细胞的miR-29 b2c进行特异性敲除。
scAAV即自互补AAV,弥补了rAAV病毒载体表达较慢的缺点,感染3天后即可表达,同时可长时间稳定表达。德国慕尼黑工业大学Stefan Engelhardt研究团队[4],利用scAAV-iCre对miR-29 b2cfl/fl 小鼠心肌细胞的miR-29 b2c进行特异性敲除。
参考文献
[1]Martinez-Lopez N, Garcia-Macia M, Sahu S, et al. Autophagy in the CNS and periphery coordinate lipophagy and lipolysis in the brown adipose tissue and liver[J]. Cell metabolism, 2016, 23(1): 113-127.
[2]Kneppers A, Verdijk L, de Theije C, et al. A novel in vitro model for the assessment of postnatal myonuclear accretion[J]. Skeletal muscle, 2018, 8(1): 1-13.
[3]Werfel S, Jungmann A, Lehmann L, et al. Rapid and highly efficient inducible cardiac gene knockout in adult mice using AAV-mediated expression of Cre recombinase[J]. Cardiovascular research, 2014, 104(1): 15-23.
[4]Sassi Y, Avramopoulos P, Ramanujam D, Grüter L, Werfel S, Giosele S, Brunner AD, Esfandyari D, Papadopoulou AS, De Strooper B, Hübner N, Kumarswamy R, Thum T, Yin X, Mayr M, Laggerbauer B, Engelhardt S. Cardiac myocyte miR-29 promotes pathological remodeling of the heart by activating Wnt signaling. Nat Commun. 2017 Nov 20;8(1):1614.
