肿瘤突变负荷(TMB),目前已成为肿瘤免疫检查点抑制剂疗效的预测生物标志物。此前,美国FDA已批准帕博利珠单抗(PD-1抑制剂)用于治疗TMB≥10个突变/Mb(简称TMB-H)的实体肿瘤。
2020年6月16日美国FDA批准F1CDx为TMB伴随诊断检测方法,2023年10月12日,南京世和医疗器械有限公司生产的“非小细胞肺癌组织TMB检测试剂盒”获NMPA批准上市。
TMB是公认的免疫治疗反应预测生物标志物。现在几乎所有的实验室都在提供TMB检测,但不同实验室在TMB的计算、报告和解释方式上存在很大差异。TMB标准化工作正在进行中,但目前还没有发表的TMB验证和报告指南。

TMB检测分析工作流程
认识到临床TMB检测所面临的挑战,美国分子病理学协会(AMP)召集美国临床肿瘤学会(ASCO)、美国病理学家协会(CAP)和癌症免疫治疗学会(SITC)组成了一个多学科TMB工作小组,基于现有证据发布了一个TMB联合共识建议,涵盖了TMB检测分析的分析前、分析中和分析后因素。随着新技术和科学的进步,应不断重新评估和修改TMB检测建议。


肿瘤突变负荷测定验证和报告的建议
该联合共识直接给出了13条专家建议,包括实验室验证分析报告,富集方法和测序panel大小等。

TMB联合共识13条建议
其中建议5 指出,实验室可以使用参考品作为TMB检测验证的补充,但不能替代临床样本。
根据实践调查结果,缺乏具有明确TMB的样本用于检测开发和验证是TMB检测实施的主要障碍。多个参考品来源(如市售质控品、细胞系、已知MSI阳性或POLE高突变样品)是可用于评估TMB准确度和精密度以及评估TMB检测分析测量范围和检测下限的。
菁良科技作为中检院TMB检测国家参考品协作单位之一,为了推动TMB这一生物标志物的研究,促进行业标准化规范化,菁良的TMB标准品能够更好地帮助IVD企业进行流程质控、试剂盒性能确认及产品注册报证等。
产品特点
● 细胞来源标准品高度模拟病人样本
● 可提供22对配对细胞系质控品用于过滤胚系突变
● 产品形式丰富:gDNA、ctDNA、FFPE蜡块
● 经过多家行业顶级检测公司测试,结果稳定一致
● 提供标准品配套完整WES数据、TMB分析流程及TMB参考值
● TMB参考值覆盖广,包含从2到28多个梯度
● 可模拟不同肿瘤细胞含量的临床样本
TMB标准品信息
|
产品类别 |
tTMB标准品、bTMB标准品 |
|
产品形式 |
gDNA、FFPE 蜡块、ctDNA |
|
参考范围及 |
可提供TMB值2到28的多个梯度TMB标准品 |
|
细胞纯度 |
肿瘤和正常配对细胞混合可提供任意AF梯度, 例 0%、10%、20%、30% |
|
验证方法 |
WES:全部类型产品 ddPCR:混合 AF 验证 |
|
WES质控参数 |
IDT xGen Exome Research Panel v1.0 捕获有效测序深度大于500X |
|
TMB参考值 |
提供WES数据及开源计算方法得到参考TMB值 |
热门产品列表
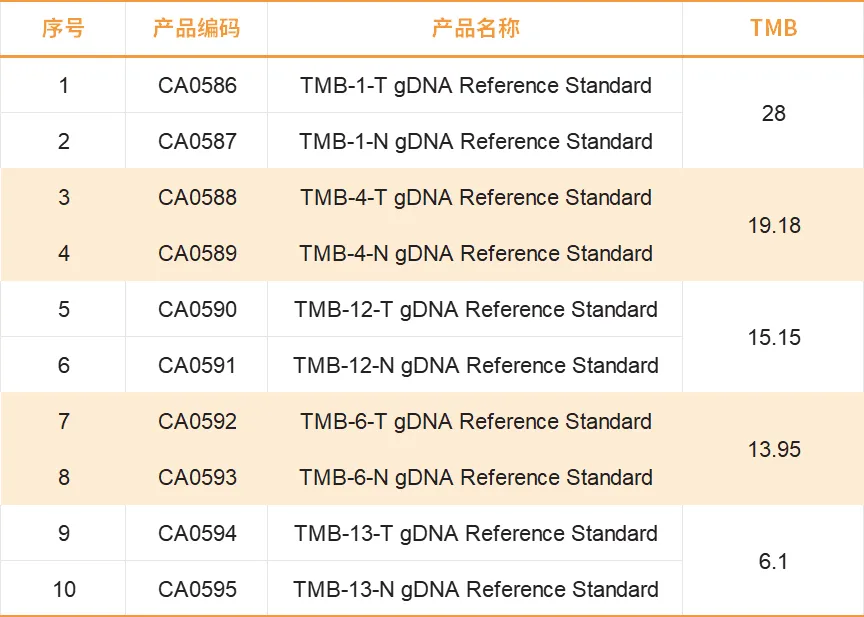
如需更多TMB参考值产品,可联系菁良客服进行定制。
|
区域 |
联系方式 |
|
东区销售负责人 |
13795223824 |
|
北区销售负责人 |
13611229766 |
|
南区销售负责人 |
15889963251 |
|
海外销售负责人 |
19804342929 |
|
全国销售总监 |
18501018000 |
|
技术支持热线 |
0755-25167057 |
