心脏是哺乳动物早期形成的器官之一,这使得它极易受到内在和外在疾病因素的影响。心肌细胞的分化受转录途径的调节,产生不同的心肌细胞群,例如窦房结细胞、房室细胞、心房细胞、心室细胞和浦肯野细胞。每个群都与特定的心脏疾病相关,因此可以通过类器官对相关疾病进行建模。3D培养心脏类器官(human cardiac organoids,hCOs)由于具有更复杂的结构和更多样的细胞类型,正在逐步成为更适用于研究心脏发育、物测试的体外模型。
本篇文章基于Nature Biotechnology【1】,Stem cells and development【2】、Development【3】、Current Protocols in Stem Cell Biology【4】发表的四篇文章,整理了人类胚胎干细胞(human ESCs)来源的心脏类器官培养方案。
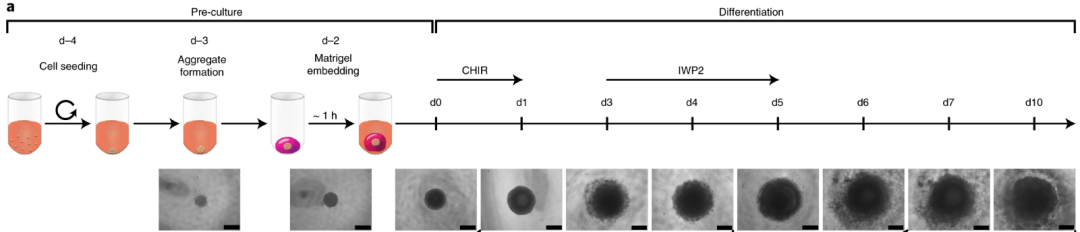
图1. hESCs来源的hCOs培养方案【1】
细胞来源
Human ESCs
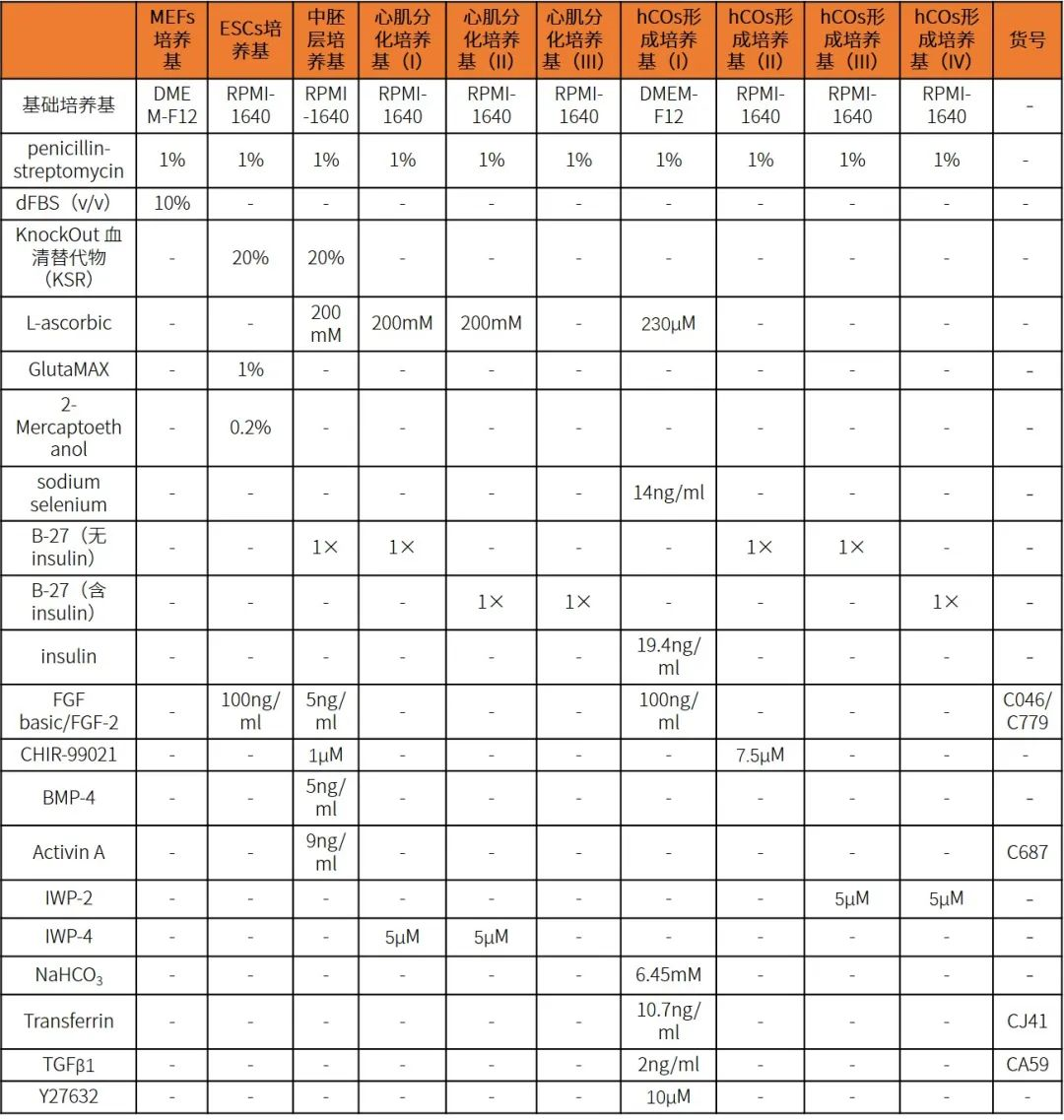
培养基配方
ESCs培养和传代
1.将100mm培养皿包被5ml 0.1%(w/v)的明胶,室温静置15min至明胶凝固。
2.在明胶上接种丝裂霉素处理过的MEFs细胞悬浮液,细胞数约为1.8×106个。放置在37℃,5%CO2的培养箱中培养至细胞汇合度70-80%时进行传代。
3.吸去MEFs培养基,将ESCs接种于明胶上,添加10ml ESCs培养基,放置在37℃,5%CO2的培养箱中培养3-5天。
4.向hESCs中加入1ml TrypLE Express,并将培养皿放置在37℃条件下进行解离,直到所有的细胞都以小细胞块或单细胞的形式漂浮。
5.将所有细胞转移至离心管中,室温下300g离心3min,收集沉淀细胞。加入DMEM-F12培养基,以1:6的比例接种在Matrigel包被的24孔培养板中,向每个孔中加入0.5ml预热的mTeSR1进行培养,在2-4天内细胞汇合度达到85-90%。
心肌分化
6.用中胚层培养基进行换液,放置在37℃,5%CO2的培养箱中培养3天,每天换液一次。
7. 用心肌分化培养基(I)进行换液,放置在37℃,5%CO2的培养箱中培养3天,每天换液一次。
8. 用心肌分化培养基(II)进行换液,放置在37℃,5%CO2的培养箱中培养7天,每天换液一次。
9. 用心肌分化培养基(III)进行换液,放置在37℃,5%CO2的培养箱中培养2天,每天换液一次。
10. 分化后,吸出原培养基,加入含 0.2% I型胶原蛋白酶和20% FBS 的PBS溶液(含Ca2+和 Mg2+),消化60min后,加入0.25% Trypsin-EDTA再消化10min。
11.加入MEM完全培养基(10%FBS,1% penicillin-streptomycin,200mM L-ascorbic)终止消化,将所得细胞用100μm孔径滤膜过滤。
hCOs培养
12. 将细胞用hCOs形成培养基(I)重悬并进行细胞计数,按照5,000个/孔的密度接种于低吸附96孔板中。4℃条件下300g离心 3 min后,放置在37℃,5%CO2的培养箱中过夜培养。
13. 用Matrigel将每孔细胞进行包埋,放置于37℃培养箱中使Matrigel固化。添加hCOs形成培养基(II)至完全没过Matrigel,放置在37℃,5%CO2的培养箱中培养1天。
14.之后用hCOs形成培养基(I)进行换液,放置在37℃,5%CO2的培养箱中培养1天。
15.用hCOs形成培养基(III)进行换液,放置在37℃,5%CO2的培养箱中培养2天后,将培养基换成hCOs形成培养基(I),放置在37℃,5%CO2的培养箱中培养1天。
16.最后用hCOs形成培养基(IV)进行换液,放置在37℃,5%CO2的培养箱中培养4-6天。
hCOs的应用和展望
hCOs是一种类似于体内器官的三维细胞结构,在很大程度上,hCOs比以前的模型更准确地保留了体内的生物学特征和功能。随着生物技术的不断发展,hCOs模型变得越来越复杂和成熟,极大地推进了心脏生理学领域的研究。
Tiburcy et al.【5】成功构建了具有心肌结构和功能特征的hCOs,通过神经体液过度刺激来模拟人类心力衰竭情况。并且在体外使用hCOs进行了药物测试,为今后针对心力衰竭开发新的治疗手段和药物提供了思路。
根据现有的报道,hCOs具有产生自发和诱发动作电位的能力,并且具有比二维模型更高的传导速度,因此hCOs可用于研究致心律失常综合征中复杂的电生理现象。Shinnawi et al.【6】使用hiPSC衍生的HCOs作为模型来评估抗心律失常候选药物的疗效。结果表明,应用奎尼丁和丙吡胺可延长动作电位持续时间,有效地缓解了心律失常。
目前hCOs仍然是相对简化的器官样组织,最重要的问题之一是缺乏丰富的血管网络等更复杂的结构。图2中的四种培养方法更好地模拟了多种细胞类型和亚区域之间的相互作用,这将有助于未来构建包含心室样和心房样结构和功能的hCOs。
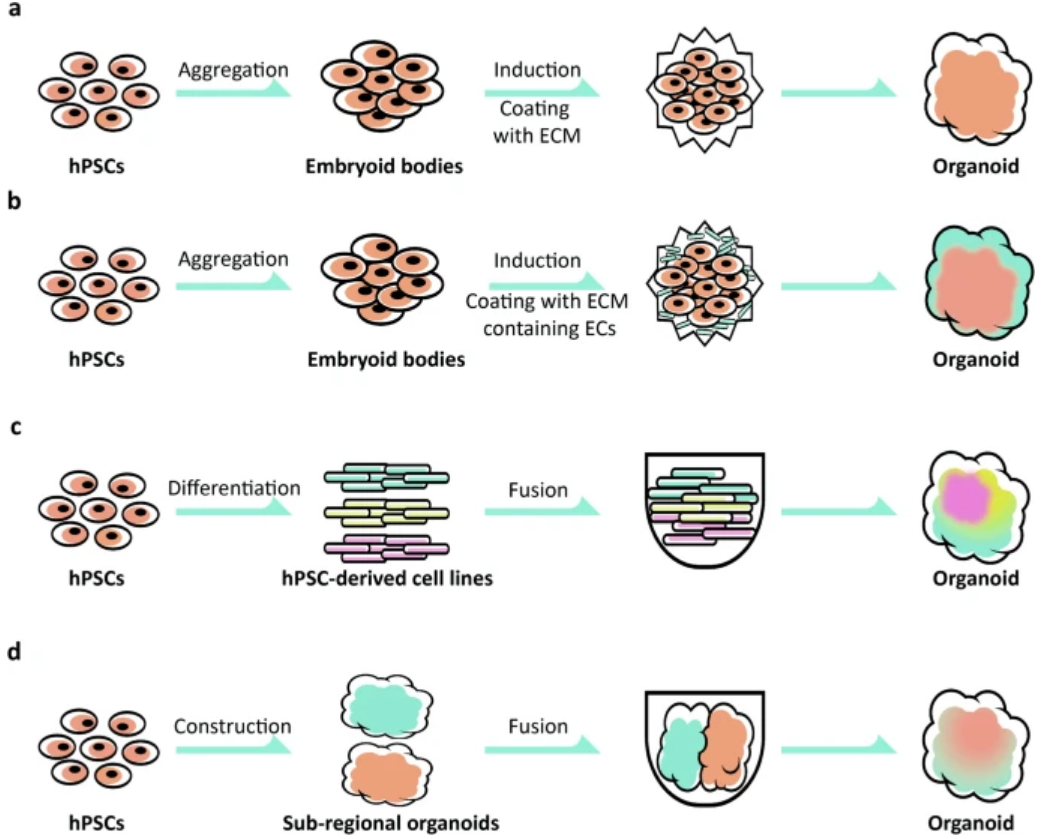
图2. 自组装hCOs形成示意图【7】
类器官作为一种研究模型,在发育生物学、疾病病理学、细胞生物学、再生机制、精准医疗以及药物毒性和药效试验等方面潜力巨大。但是,类器官培养技术建立过程中会面临多种挑战。为了更轻松更高效的建立类器官培养技术,欢迎各位扫码加入类器官培养交流群,在这里会有专业的技术支持人员帮您解惑答疑,也将定期分享类器官前沿进展,让类器官培养更简单!

类器官培养交流群
推荐产品-心脏类器官培养
|
货号 |
产品名称 |
|
Human/Mouse/Rat Activin A |
|
|
Human FGF basic/FGF-2 |
|
|
Mouse FGF basic/FGF-2 |
|
|
Human TGF-beta 1 |
|
|
CJ41 |
Human Transferrin |
相关产品:
|
货号 |
产品名称 |
|
Human/Mouse/Rat BDNF |
|
|
Human/Mouse/Rat BMP-2 |
|
|
Human DKK1 (N-8His) |
|
|
Human EGF |
|
|
Mouse EGF (C-6His) |
|
|
Human FGF-4 |
|
|
Mouse FGF-4 |
|
|
Human FGF-7/KGF |
|
|
Human FGF-9 |
|
|
Mouse FGF-9 (N-6His) |
|
|
Human FGF-10 |
|
|
Human FGF-19 (N-6His) |
|
|
Human GDNF |
|
|
Human HGF (C-6His) |
|
|
Mouse HGF (C-6His) |
|
|
Human LIF |
|
|
Mouse LIF |
|
|
Human Noggin |
|
|
Mouse Noggin(C-6His) |
|
|
Human NRG1-beta 1 |
|
|
Human NT-3 |
|
|
Human OSM (N-6His) |
|
|
Human Prolactin/PRL |
|
|
Human R-Spondin 1 (C-6His) |
|
|
Human R-spondin 3 (C-Fc-6His) |
|
|
Human Shh |
|
|
Human Shh (C24II) |
|
|
Mouse Shh |
|
|
Mouse Shh(C25II) |
|
|
Human Wnt3a |
|
|
Human Wnt3a V2 |
参考文献
【1】Drakhlis, L. et al. (2021). Human heart-forming organoids recapitulate early heart and foregut development. Nature Biotechnology, 39(6), 737-746.
【2】Hudson, J. et al. (2012). Primitive cardiac cells from human embryonic stem cells. Stem cells and development, 21(9), 1513-1523.
【3】Voges, H. K. et al. (2017). Development of a human cardiac organoid injury model reveals innate regenerative potential. Development, 144(6), 1118-1127.
【4】Costa, M. et al. (2008). Expansion of Human Embryonic Stem Cells In Vitro. Current Protocols in Stem Cell Biology, 5(1), 1C-1.
【5】Tiburcy, M. et al. (2017). Defined engineered human myocardium with advanced maturation for applications in heart failure modeling and repair. Circulation, 135(19), 1832-1847.
【6】Shinnawi, R. et al. (2019). Modeling reentry in the short QT syndrome with human-induced pluripotent stem cell–derived cardiac cell sheets. Journal of the American College of Cardiology, 73(18), 2310-2324.
【7】Zhao, D. et al. (2021). Cardiac organoid—A promising perspective of preclinical model. Stem Cell Research & Therapy, 12(1), 1-10.
苏州近岸蛋白质科技股份有限公司,是一家专注于重组蛋白应用解决方案的高新技术企业,主营业务为靶点及细胞因子类蛋白、重组抗体、酶及试剂的研发、生产和销售,并提供相关技术服务。公司定位为医疗健康与生命科学领域原料与技术解决方案的上游供应商,致力于为下游客户提供及时、稳定、优质的产品及服务,助力全球生物医药企业和研究机构的技术与产品创新升级。
详询www.novoprotein.com.cn或致电400-600-0940。
