2023年8月1日,中国合格评定国家认可委员会发布《关于发布CNAS-CL02-A001:2023〈医学实验室质量和能力认可准则的应用要求》和CNAS-EL-14:2023《医学实验室认可受理要求的说明〉的通知》。该文件将代替CNAS-CL02-A001:2021《医学实验室质量和能力认可准则的应用要求》,并于2023年12月1日起正式实施。
其中关于检验结果的有效保证对于室内质量控制的要求如下:
1、宜参考相关国家/行业标准建立质量控制程序,如 WS/T 641,内容包括:质控规则(质控规则应确保试验的稳定性和检验结果的可靠性);质控物的类型、浓度和检测频度;质控物位置(如酶联免疫试验,适用时,用质控物应随机放置且应覆盖检测孔位);质控记录。
2、质控物可为商品化质控物或自制质控物。
3、定量检测项目:
应至少使用两个浓度水平(正常和异常水平)的质控物。可利用质控图对质控数据进行统计分析,包括失控时的分析处理程序和纠正措施等。
4、定性检测项目:
每次实验应设置阴性、弱阳性和/或阳性质控物,并对质控数据进行分析,包括阴、弱阳性和/或阳性结果是否符合预期。
5、病理实验室:
a) 应制定科内疑难病例讨论制度,每月至少 1 次;
b) 应监测检查结果与既往病理诊断的符合率、术中冰冻和石蜡切片诊断的符合率;
c) 应定期随机抽取病理报告进行内部同行复阅;
d) 应建立细胞和组织学病理报告结果对照的统计分析制度。
e) 应建立妇科细胞学结果统计分析制度,如不满意、阴性、非典型、低级别及高级别病变的比例等各种病变的比例。
6、分子诊断实验室:
a) 若开展核酸提取,适当时,应评价核酸的含量和质量(如纯度和完整性)并保留评价记录。
b) 若开展基因变异、基因多态性或基因型检测,质控物应宜包括临床常见的或者是最具临床价值的变异类型或者基因型。
c) 若开展肿瘤组织分子病理检测应评估样品中肿瘤细胞的含量并记录。
7、微生物实验室:
应至少对使用中的染色剂、凝固酶、过氧化氢酶、氧化酶及抗菌药物敏感性试验等进行质量控制。应贮存与诊断相配套的质控物,以便在染色、试剂、试验、鉴定系统和抗菌药物敏感性试验中使用。药敏用标准菌株种类和数量应满足工作要求,保存其来源、传代等记录,并有证据表明标准菌株性能满足要求。
参考文献:CNAS-CL02-A001:2023《医学实验室质量和能力认可准则的应用要求》
菁良临床质控一站式解决方案
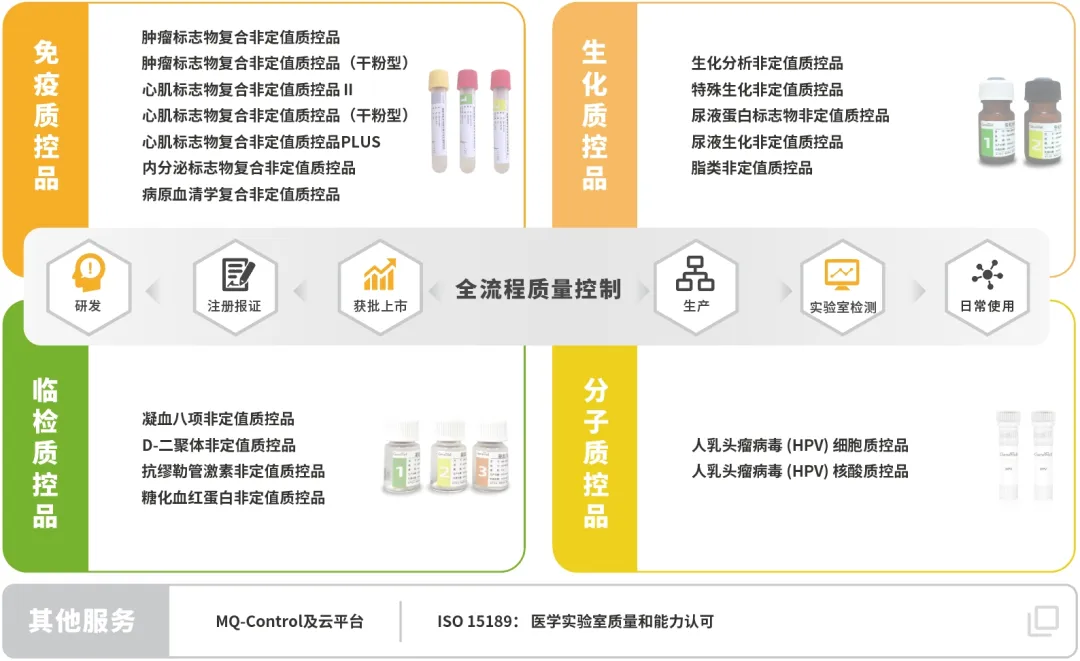
关于菁良
菁良科技(深圳)有限公司是全球领先的提供体外检测标准品的研发创新型高科技企业。
体外检测需要标准品!随着经济的快速发展,科技细分领域的不断拓展,国民生活水平的不断提高,检验检测市场需求也随之快速上升,体外检测进入高速发展阶段。然而配套的质量控制和规范化意识却相对滞后,很大一部分体外检测方法仍然存在效率低下且检测准确率有限的情况。菁良通过自主研发的高科技平台,向体外检测行业用户及合作伙伴提供全球领先的标准物质、第三方质控产品和研发参考品服务,助力提高行业检测准确率!
菁良自2018年成立以来,始终以推动行业规范化、标准化为己任,参与多项由检测领域行业龙头发起的标准制定工作,多次支持由临检中心发起的室间质量评价 (EQA)/能力验证项目。菁良拥有全球领先的标准品研发技术和资深的国际拓展经验,已推出众多行业首创的参考品和第三方质控品,被广泛用于检测试剂和仪器的工艺开发、以及检测过程之中。菁良秉承着“菁准智标,匠心良造”的理念,怀抱着“提高体外检测准确率,助力精准医学快速发展”的愿景,致力于建立规范化的中国体外检测金标准平台。
